心血管疾病是目前人类的头号死因,每年死于心血管疾病的人数多于任何其它病因。心力衰竭是所有心血管疾病的终点。造成心力衰竭的原因有很多,高血压和血栓等病理性刺激导致的心肌肥大就是一个重要诱因。要避免走到心力衰竭这一步,抑制和逆转病理性心肌肥大以及延缓心肌重构的发展就尤为重要。尽管市面上已经有很多药物可以治疗心血管疾病,但心衰领域仍存在可用药物较少、疗效不足、药物副作用引起的用药安全性问题等。因此,新靶点的发现和创新药物研发迫在眉睫。
浙江大学医学院、良渚实验室张岩教授课题组联合北京大学基础医学院张岩教授课题组合作开展研究,基于结构精准设计了有效改善心肌肥厚的apelin受体调节剂,为精准靶向改善心血管疾病药物开发提供了全新策略。
北京时间2024年3月1日,该成果发表在国际顶级期刊《细胞》上。浙大张岩与北大张岩为论文共同通讯作者。浙江大学博士后王伟伟、博士生戢素玉、北京大学基础医学院博士生张文佳、北京大学第三医院博士后张俊霞、浙江大学博士生蔡晨曦、强基计划本科生胡如碧为共同第一作者。

APLNR的两面性
G蛋白偶联受体(GPCRs),顾名思义是一个“和G蛋白连接才能工作的受体”,它定位于细胞膜上并参与大部分生理功能的调节,常被作为药物靶点来进行研究。Apelin是A类G蛋白偶联受体(APLNR)的内源性配体,可同时激活APLNR下游的G蛋白和β-arrestin信号通路,调节多种生理病理过程。特别是在心血管系统中,APLNR激活可促进血管舒张、正性肌力、血管生成、利尿、降低血压等,还参与心血管疾病的病理生理调节,如抑制心肌纤维化、减轻病理性心肌肥厚、抵抗心力衰竭和肺动脉高压等,因此被认为是极有前景的心血管疾病干预靶点。但是,内源性配体apelin诱导的心脏保护效应主要归因于其中的G蛋白信号,而其同时激活β-arrestin信号反而会对健康心脏引起有害的心肌肥厚,削弱药效。
正是这样的“两面性”让科学家们犯了难,正向效应和负面作用并存,严重影响了药物的有效性和安全性。多家国际知名药企和科研机构都在尝试开发安全有效的APLNR激动剂类药物,但至今仍未有精准靶向药物分子获批上市。
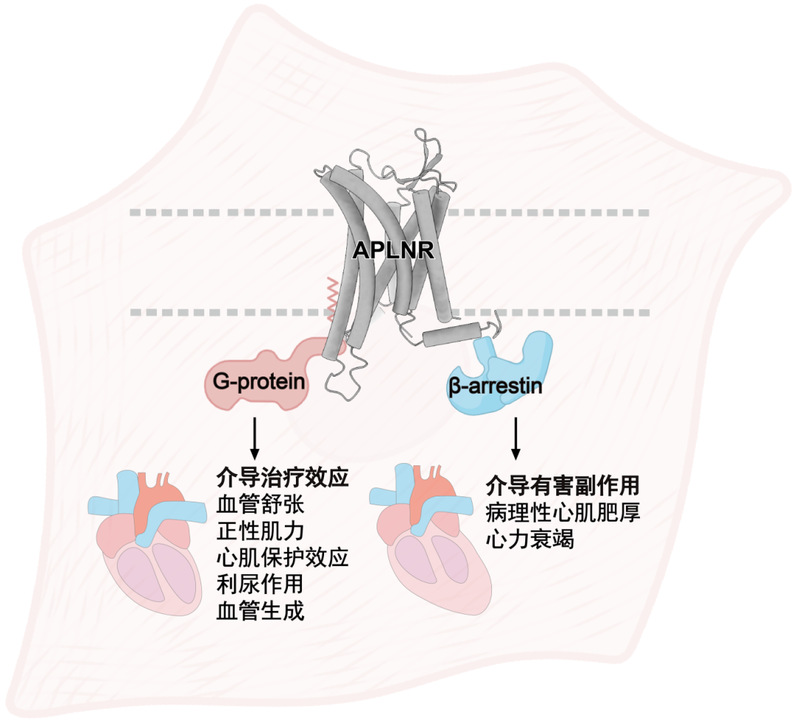
APLNR介导的下游信号及病理生理功能
浙江大学张岩教授团队长期致力于跨膜信号转导的机制研究和精准调控手段设计,发展并奠定了基于冷冻电镜的GPCR药理学研究方法,在基于结构设计精细调控GPCR功能的先导分子并实现疾病的精准干预方面取得了系列创新成果。北京大学张岩教授团队一直以来聚焦于心肌损伤的机制及其在心血管疾病中的作用,针对性研发疾病防治靶点和干预手段,为临床心血管疾病的预防与治疗提供新策略。
同名同姓的两位学者开始了接力合作研究。
阳关道还是独木桥?
研究的第一步是揭开不同信号谱激动剂是如何激活受体介导下游信号的奥秘。
团队把三种激动剂摆在一起“找不同”,借助冷冻电镜,解析了内源性平衡激动剂apelin,两种部分G蛋白偏向性激动剂MM07和CMF-019识别APLNR与下游Gi1蛋白复合物的高分辨率结构。结果发现,这三种激动剂结合的APLNR-Gi1复合物长得非常像,就好比是“三胞胎”,外观上似乎并没有什么差别。
课题组没有放弃,经过实验再三甄别,终于看到了其中的细微差异。如果把配体比作一把钥匙,受体比作锁,apelin的顶端也就是钥匙的钥匙柄是相对伸展的,MM07这把钥匙的钥匙柄弯曲成环状,这导致了它们的钥匙主体部分插入受体锁芯的深度和具体位置各有差异,他们将钥匙主体部分的关键部位,M11和F13插入的两个口袋定义为“双热点”,这是影响偏向性信号转导的关键。

三种激动剂结合的APLNR-Gi1复合物冷冻电镜结构比较并定义“双热点”
这个差别由配体结合口袋传递到下游效应蛋白结合口袋的信号转导机制,发生了关键的变化——其中位于极性网络中心的D752.50作为一个偏向性信号的开关,产生了0.1纳米的结构偏移。正是这只有头发丝直径百万分之一的空间位置差别,导致下游效应蛋白结合口袋的不同构象重排,最终决定了是激活G蛋白信号还是激活β-arrestin信号。
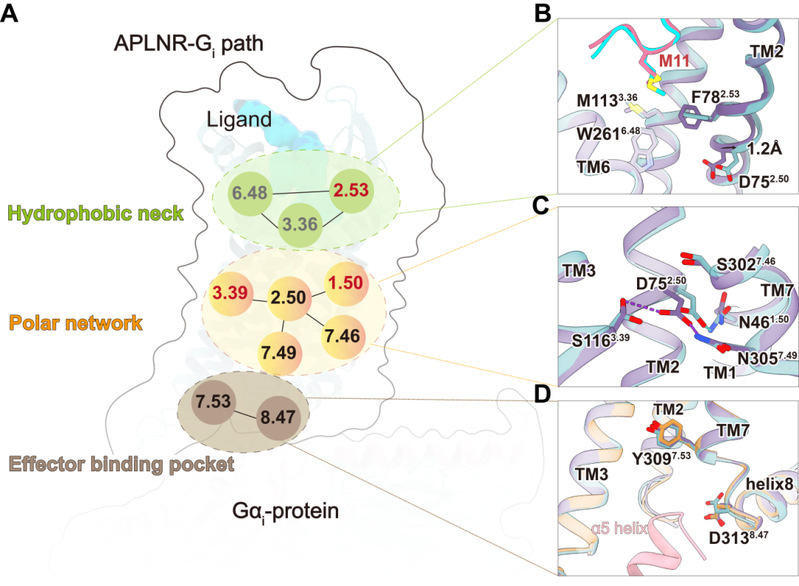
信号通过极性网络向胞内传递
浙大张岩教授说:“在揭示了不同偏向性信号分子识别并激活APLNR的分子机制后,我们针对性地设计了绝对的G蛋白偏向性激动剂WN353和WN561,在消除β-arrestin活性的同时保持了G蛋白信号转导能力。”
“盲选”验证 有望“定制”靶向药物
为了避免干扰,团队把新设计的激动剂和市面已有激动剂混在一起打乱编号,利用体外培养心肌细胞和在体心脏疾病动物模型进行“双盲”功能筛选和验证。王伟伟博士说:“召开‘揭盲’线上会议时,心情万分紧张。结果完美显示我们设计的完全G蛋白偏向性激动剂WN353和WN561完全没有导致心肌肥大的副作用。我们的实验也再次证明了,APLNR的β-arrestin信号通路确实是导致心肌肥大的主要通路”。
随后研究者又模拟了存在心肌肥大但没有病理刺激的情况下APLNR激动剂的治疗效果,如患有瓣膜疾病或高血压的患者。结果证实Apelin加剧了心肌肥大,而MM07和CMF-019没有效果。令人振奋的是,新开发的激动剂WN561在有或没有病理刺激的条件下都可以改善小鼠心肌肥大,进一步证明了这种新型G蛋白完全偏向的APLNR激动剂在治疗心肌肥大和心力衰竭中的前景。

新型完全APLNR偏向激动剂WN561的设计理念及心肌保护活性效果
该项研究工作揭示了APLNR与不同偏向性配体复合物的识别特征,首次成功理性设计了绝对G蛋白信号选择性的APLNR激动剂。通过三种动物模型展示了新设计活性分子的安全性和有效性,为靶向APLNR的改善心血管疾病药物开发提供了全新策略。

浙大张岩课题组部分研究人员合影
浙大张岩说,也许在不久的未来,就可以“定制”出能让心肌“减肥又增效”的药物,帮助心血管病人重新“心花怒放”。
(文 吴雅兰/声像 杨萝萝 科研图片由受访团队提供)
