T细胞和自然杀伤(NK)细胞协同维持免疫稳态。目前的癌症免疫疗法主要依赖于这些细胞的个体应用。
2025年7月14日,浙江大学基础医学院孙洁、黄河共同通讯在Nature Biomedical Engineering(IF=26.6)在线发表题为“Bispecific killer cell engager-secreting CAR-T cells redirect natural killer specificity to enhance antitumour responses”的研究论文,该研究开发了一种分泌双特异性杀伤细胞接合器的CAR-T细胞,重定向自然杀伤特异性以增强抗肿瘤反应。
该研究使用双顺反子载体来共表达嵌合抗原受体(CARs)和分泌型免疫细胞接合子(ICEs),利用两种效应细胞类型的联合治疗潜力。在体外验证了免疫细胞接合物的分泌和功能后,在小鼠模型中系统地比较了各种组合方法,确定了分泌双特异性杀伤细胞接合器(BiKE)的CAR-T细胞和NK细胞的高效组合。除了常规CAR-T细胞和NK细胞的简单组合之外,该策略在CD19+ B细胞白血病和淋巴瘤以及EGFR+实体瘤模型中表现出优异的功效,同时降低了对CAR-T细胞的剂量依赖性。此外,靶向不同抗原的CAR-T细胞和BiKEs表现出对具有异质抗原表达的肿瘤细胞的抑制。这些发现表明,将分泌BiKE的CAR-T细胞和NK细胞结合起来提供了一种对抗肿瘤抗原异质性和免疫逃避的有前途的策略。

T细胞和NK细胞依靠不同的识别机制来清除恶性细胞。然而,肿瘤细胞已经进化出各种方式来逃避这些免疫效应细胞(IECs)的免疫监视,包括抗原丢失和抗原呈递缺陷,抑制性配体的上调和活化配体的下调。在这种情况下,重定向免疫识别已成为一种有效的方法,可绕过T细胞的主要组织相容性复合体(MHC)限制,并赋予NK细胞抗原特异性,从而释放其治疗潜能。目前广泛使用两种类型的免疫重定向:表达特异性嵌合抗原受体的IECs基因工程,以及通过双特异性或三特异性抗体使IECs与肿瘤细胞结合。这两种重定向方法在临床上表现出令人兴奋的抗肿瘤效果,因此成为癌症免疫治疗的焦点。
靶向CD19和B细胞成熟抗原的CAR-T细胞已在B细胞恶性肿瘤患者中获得临床成功,包括B细胞白血病和淋巴瘤以及多发性骨髓瘤。值得注意的是,这些“活药”一旦投放,就能形成免疫记忆,甚至在十年后仍能对肿瘤细胞进行巡逻和监视。然而,生产成本昂贵,生产周期漫长,同种异体T细胞需要广泛的工程改造来减轻移植物抗宿主病(GvHD)和宿主排斥反应,这些问题阻碍了CAR-T细胞疗法的广泛应用。除了CAR介导的免疫重定向外,另一种方法是通过双特异性或三特异性抗体识别肿瘤抗原并同时激活效应细胞,使T细胞或NK细胞与肿瘤细胞结合。到目前为止,FDA已经批准了12种双特异性抗体,其中大多数针对CD3以重定向内源性T细胞。
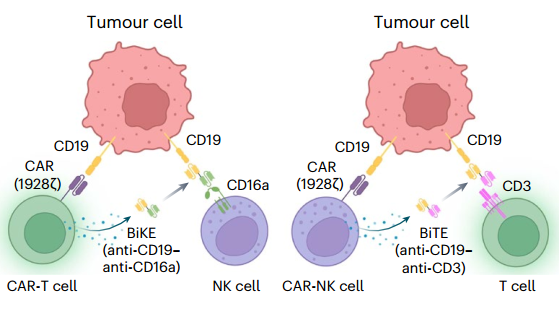
机理模式图(图源自Nature Biomedical Engineering)
尽管基于T细胞或NK细胞的单一疗法已经显示出希望,但它们经常遇到局限性。与此同时,很少有人试图将它们结合起来加以利用。虽然CAR-T细胞疗法已经与各种模式相结合,包括化疗、放疗和免疫检查点抑制剂(ICI),但其与NK细胞的整合仍未得到探索。在该研究中,通过携带第二代CAR编码序列和分泌型杀伤细胞接合剂的双顺反子载体,将CAR和BiKE介导的T细胞和NK细胞免疫重定向的整合概念化。BiKE分泌的CAR-T细胞和BiKE参与的NK细胞在血液系统恶性肿瘤和实体瘤的动物模型中协同显示出优异的体内抗肿瘤疗效,表明了这一策略的转化潜力。



