结束一场紧张的考试,写完一份棘手的报告,当你坐下来听着音乐放松一下时,你的大脑其实还处于压力之中——生活中我们会遇到各种压力,大脑的应激并不会在压力解除时立刻停止。就像在平静的湖面投入一块石头,涟漪要过一段时间才渐渐消失。
通过追踪压力在大脑中的“涟漪”,胡海岚团队发现:大脑中有一个“压力电台”,它有三位“主播”坐镇:外侧缰核(LHb)神经元、蓝斑核(LC)去甲肾上腺素能神经元和LHb星形胶质细胞。当压力来临,三位“主播”跨脑区联动“播送”压力信息。经过LHb星形胶质细胞的推波助澜,短暂的压力刺激转化为持续时间更长的神经元活动。这种独特的响应机制为长期压力积累触发抑郁情绪埋下了隐患。

相关研究论文Neuron-astrocyte Coupling in Lateral Habenula Mediates Depressive-like Behaviors于4月24日发表在Cell杂志。该研究向人们展示了不同细胞类群协同参与情绪编码的图景,从分子、细胞和神经环路水平解释了“压力山大”导致抑郁的原因。在临床上,该项研究有望为我们进行压力管理、抑郁预防和治疗提供新的靶点。浙江大学医学院胡海兰教授为通讯作者,浙江大学医学院博士生辛倩倩、王俊盈为共同第一作者。
“星星”在闪烁
缰核(Habenula)是脊椎动物大脑中的“标配”核团。其中外侧缰核(LHb)素有“反奖赏中心”之称,当我们遇到压力、恐惧、挫败时,这个脑区就会激活,参与负面情绪的编码。在这里追踪压力的传播轨迹时,胡海岚研究团队决定观察一片陌生的“风景”——星形胶质细胞。胡海岚说:“过去关于LHb的研究普遍集中在神经元,而很少关注到星形胶质细胞。它们在做什么,是如何与神经元互动的,我们还知之甚少。”
人类大脑中,星形胶质细胞约占脑细胞总数的40%。由于它们不会像神经元那样放电,最初人们认为它们就像“胶水”,只是为神经元提供保护和支撑,而并不参与大脑的复杂功能。直到最近30年,这片大脑中的“小透明”才引起科学界的关注,它们的“隐藏技能”被陆续发掘,例如,参与调节神经元突触的发育,调节神经元的可塑性等。
当星形胶质细胞工作时,细胞内的钙离子浓度会显著变化,于是我们能以钙离子信号来判断它们的动静。然而,LHb是一个既小又致密的核团,从前还没有人观察过这个脑区的星形胶质细胞。研究人员摸索了多种病毒工具和成像参数,得到了一张又一张漆黑一片的“废片”后,终于让钙信号从一片嘈杂的信息中清晰地显现出来。
“它们就像星星在夜空闪烁。”论文共同第一作者,博士生辛倩倩记得第一次看到信号时的激动,“星形胶质细胞并不‘沉默’,相反,它们还非常活跃!” 论文共同第一作者,博士生王俊盈介绍,他们同时监测了多个脑区的星形胶质细胞的动静,当漫步中的小鼠遭遇脚底一麻,LHb星形胶质细胞反应最快,它们是大脑中最先承接压力的星形胶质细胞。
三群细胞一台“戏”
人类社会中,频繁的、持续的压力是抑郁的最常见诱因。胡海岚团队2018年发表在Nature的一项工作指出,抑郁样行为源自大脑LHb神经元的簇状放电。但当时他们并不知道这些神经元为什么出现了异常。于是团队决定追溯:最初的压力对神经元“做”了什么?星形胶质细胞是否参与其中?
研究团队设计了动物实验,用1秒钟随机的足底电击给小鼠制造一次压力,然后“偷听”LHb的脑细胞“说话”:首先传来一波神经元的信号,间隔一秒之后,星形胶质细胞的信号紧随其后。“这提示前者可能参与主导后者的活动,但滞后响应的星形胶质细胞怎么影响先前的神经元活动呢?”胡海岚的提问让让辛倩倩猛然意识到,她应该在更长的时间尺度上去观察神经元的活动:“我们发现LHb神经元在第一次强烈激活后,其实还有第二次激活。”辛倩倩介绍,当他们把观察时间从5秒延长到50秒,才看到了这种从未被报道过的“神经余震”,它虽然信号微弱,但持续时间长。
“对话记录”显示,星形胶质细胞的信号恰好卡位在神经元的两次活动之间。正当研究团队想就此“结案”,将压力应激描述为LHb内神经元和星形胶质细胞的互动时,实验环节又出了意外:在离体脑片实验中,LHb的神经元并不能“唤醒”星形胶质细胞。激活LHb胶质细胞另有其“人”?这个意外迁出了“压力对话”中的另一位主角——蓝斑核(LC)去甲肾上腺素能神经元,它的“特产”去甲肾上腺素才是激活LHb星形胶质细胞的幕后推手。
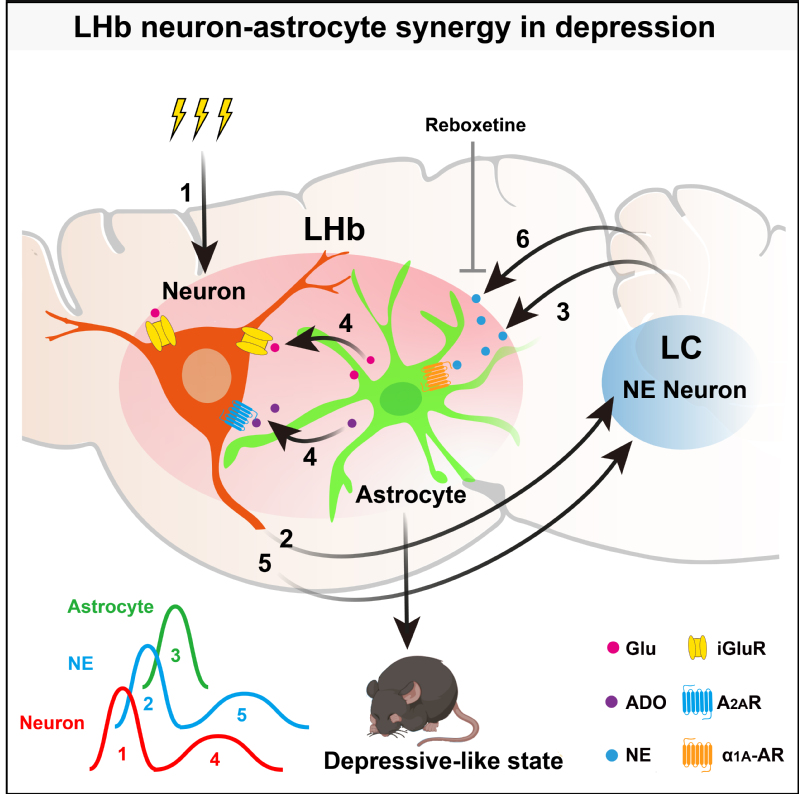
经过一连串实验摸索,压力在大脑中的传播路径逐渐完整,大脑深处的“压力电台”也随之浮出水面,这是神经元与星形胶质细胞之间独特的双向“对话”:压力来临时,LHb神经元最早“觉醒”,它随即远程“唤醒”LC去甲肾上腺素能神经元释放去甲肾上腺素(NE);当NE到达LHb脑区,LHb星形胶质细胞被激活加入“对话”,释放胶质递质。这引起了LHb神经元的第二次长时程的活跃。——压力信号就像一个回旋镖,从LHb神经元出发,到LC脑区转了一圈后又回到LHb脑区,由星形胶质细胞传回给LHb神经元。
“压力电台”与抑郁
胡海岚说,神经科学领域中长期存在一个重要的科学问题:为什么神经元能在短暂的外界刺激后持续活动?过去的理论主要归因于神经调质的缓慢作用或者神经元网络的循环作用。在胡海岚团队的小鼠实验中,短短1秒钟的压力刺激引发了LHb神经元和去甲肾上腺素信号长达1分钟左右的持续活动。这种独特的“神经余震”现象,引导研究团队发现了一种全新的机制:星形胶质细胞的参与。在一次压力响应的“对话”中,占据“C位”的星形胶质细胞推动了神经元的第二次长时程激活。
“了解大脑是如何响应压力的,有助于我们更好地理解抑郁。”胡海岚说。在动物行为实验中,随机20次左右的压力刺激引发了小鼠的抑郁样行为。研究团队指出,正是由于压力频繁激活了“压力电台”,使其不堪重负,最终促发了LHb神经元的活动异常。
研究团队认为,可以通过调控LHb星形胶质细胞来调整压力对大脑的影响:当研究人员激活小鼠LHb星形胶质细胞,它们的心理防线似乎明显变弱,少数几次的压力刺激下就产生了抑郁情绪。而当研究人员定向“关闭”LHb星形胶质细胞,在超过了压力刺激阈值的情况下,小鼠也照样情绪稳定。“我们在实验中发现了调控星形胶质细胞活动的分子和相关受体,它们有潜力成为调控抑郁的靶点。”胡海岚说。
双面“压力分子”
当我们以分子的角度“观看”压力在大脑中的传递,会发现一个有趣的分子——去甲肾上腺素(NE)。没错,它就是著名的“压力分子”——肾上腺素在大脑中的版本,那个在考试时助你才思泉涌,赛跑时超常发挥的分子。压力应激时,LHb神经元远程调动蓝斑核神经元分泌去甲肾上腺素并向全脑输送。
当前,神经科学领域对NE的认识还很矛盾:五羟色胺-去甲肾上腺素再摄取抑制剂(SNRIs)和去甲肾上腺素再摄取抑制剂(NRIs)作为经典的抗抑郁药物,在临床上展示出显著的的抗抑郁效果。这些药物会阻断NE的回收,提升细胞外NE的浓度,因此有假说提出抑郁症是由于大脑中缺乏NE;与之矛盾的是,抑郁症患者的脑脊液和血液中的NE水平都有异常升高的现象。
“在我们研究的压力介导抑郁情绪的动物模型中,NE也是升高的。”胡海岚指出,其中原因在于:压力应激会介导两种NE的释放模式,一种是瞬时的强烈释放;另一种是缓慢的持续释放。只有前者才能‘撼动’LHb 星形胶质细胞。SNRIs 和NRIs增加了缓慢释放的量,反而让NE的瞬时释放受阻。“在NE瞬时释放受阻的情况下,星形胶质细胞无法完成压力传导,进而阻断了压力信号的扩散。”辛倩倩说,这为厘清临床用药中的一对矛盾提供了合理的解释,为优化相关用药手段提供了启发。

生活中,我们常与压力不期而遇。这项研究告诉我们,在压力事件解除后,大脑还需要一段时间才能缓过劲来。“消化”压力需要时间或者方法。“要想办法阻断压力的累积。”胡海岚说,科学研究常常让人暴露在压力之中,特别是摸索星形胶质细胞的成像和操纵工具阶段,是团队成员压力最大的阶段。实验攻关期间,两位博士生常常并肩坐在实验台前实验、观察到凌晨,相互鼓劲。王俊盈还把一双圣诞袜挂在实验台上,在实验受挫时对它许愿:“下一张脑片,一定要成功!”
(文 周炜/图 由课题组提供)



