腹膜转移瘤是一种十分常见且致命的肿瘤转移类型,患者中位生存期只有6-9个月,多继发于腹腔内肝、胃、结肠、胰腺和卵巢的癌种和腹膜后的恶性肿瘤。细胞减灭术,也即手术治疗,是临床治疗腹膜转移瘤的主要手段,但这类侵入性治疗往往会造成一系列术后并发症,如肿瘤的复发及二次转移、腹腔粘连等等,严重影响患者生存质量,并导致差的预后。目前在临床上仍缺少有效手段对上述并发症进行干预。
2024年4月18日,浙江大学基础医学院周泉/刘祥瑞/周天华在《Advanced Materials》杂志发表了题为“Neutrophil Extracellular Traps-Inhibiting and Fouling-Resistant Polysulfoxides Potently Prevent Postoperative Adhesion, Tumor Recurrence and Metastasis”的研究文章。发布了一种含有亚砜结构的新型生物医用材料,该材料在体内外多种模型中,均能显著抑制包括腹腔粘连、肿瘤转移和复发等多种术后并发症。

术后的急性炎症环境是导致多种并发症产生的主要原因。手术过后,中性粒细胞作为主要的炎症响应细胞会迅速迁移至术后炎症部位,中性粒细胞中的髓系过氧化物酶(myeloperoxidase,MPO)能在短时间内催化过氧化氢(H2O2)氧化生成强氧化性次氯酸(HOCl),损伤组织,从而加剧炎症进程。同时,近年越来越多研究表明,中性粒细胞还会通过“NETosis”这种特有的死亡方式,释放出中性粒细胞胞外陷阱网(NETs),加剧肿瘤复发、转移等并发症的形成。因此,调节术后炎症微环境、抑制NETs的过度释放有望同时干预上述病理过程。
亚砜结构是一类安全、具有生物活性的化学基团,该基团能够和水形成强氢键,具有强亲水性;同时又能被继续氧化成亲水性较弱的砜或者还原成疏水性硫醚,因此具有良好的氧化还原调节能力。自然界中存在着大量的含有亚砜基团的天然小分子生物活性物质,如二甲基亚砜(DMSO)、莱菔子素(sulforaphane)等,其都发现具有潜在的抗炎、镇痛、皮肤渗透增强剂等功能。受此启发,研究者设计合成了一系列含亚砜基团的丙烯酸酯均聚物(图1),通过筛选发现聚合物PMeSEA具有超亲水性,在体内外均表现出显著优于聚乙二醇(PEG)的抗蛋白/细胞吸附活性,能显著抑制多种细胞的定植。
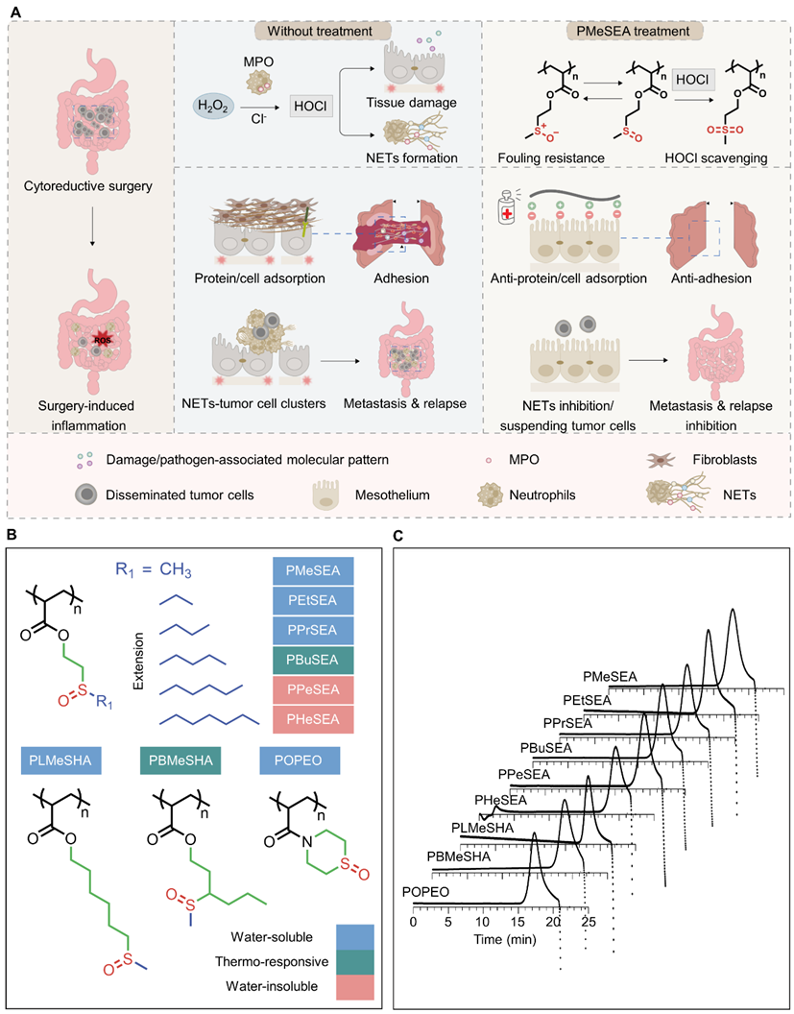
图1 亚砜均聚物结构及筛选得到PMeSEA预防术后并发症的示意图
不仅如此,由于PMeSEA不能被正常细胞或者组织内的H2O2氧化,而只能被炎症性免疫细胞如中性粒细胞、巨噬细胞产生的HOCl氧化,因此PMeSEA够选择性清除炎症性细胞产生的组织破坏性的HOCl,而不影响正常细胞内H2O2水平,从而降低炎症,并减少对正常细胞氧化还原平衡的扰动(图2)。
鉴于NETs的释放依赖MPO酶的活性及其产生的HOCl稳定其网状结构,进一步研究发现,PMeSEA在清除中性粒细胞的HOCl后,进一步显著抑制了其NETs的释放(图3)。
之后,作者建立了包括盲肠-腹壁粘连模型以及缺血纽扣等粘连模型,发现PMeSEA能够有效阻止腹腔粘连的发生(图4)。接着建立了肿瘤腹膜转移和肺转移模型,发现腹腔注射PMeSEA能有效抑制肿瘤腹腔转移,而尾静脉注射其能够有效抑制肿瘤肺转移(图5)。最后,作者构建了模拟临床细胞减灭术手术的术后复发模型。发现PMeSEA能同时抑制腹膜肿瘤复发和腹腔粘连等多种术后并发症。进一步的体内安全性实验表明,PMeSEA具有良好的生物安全性,揭示了其作为术后干预生物材料的突出潜力。
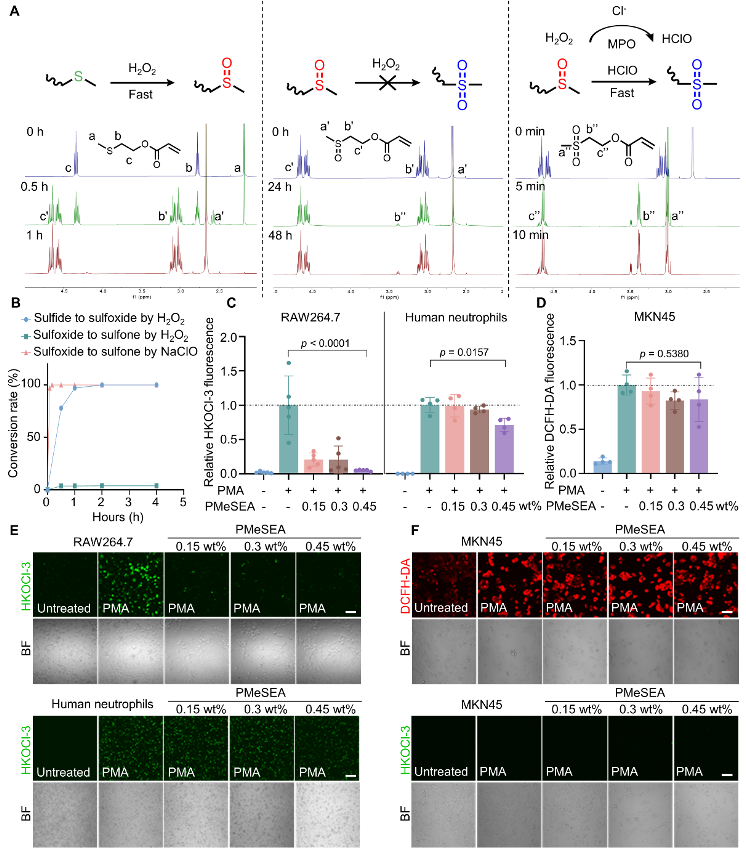
图2 PMeSEA选择性清除炎症细胞(巨噬细胞或者中性粒细胞)产生的组织破坏性HOCl
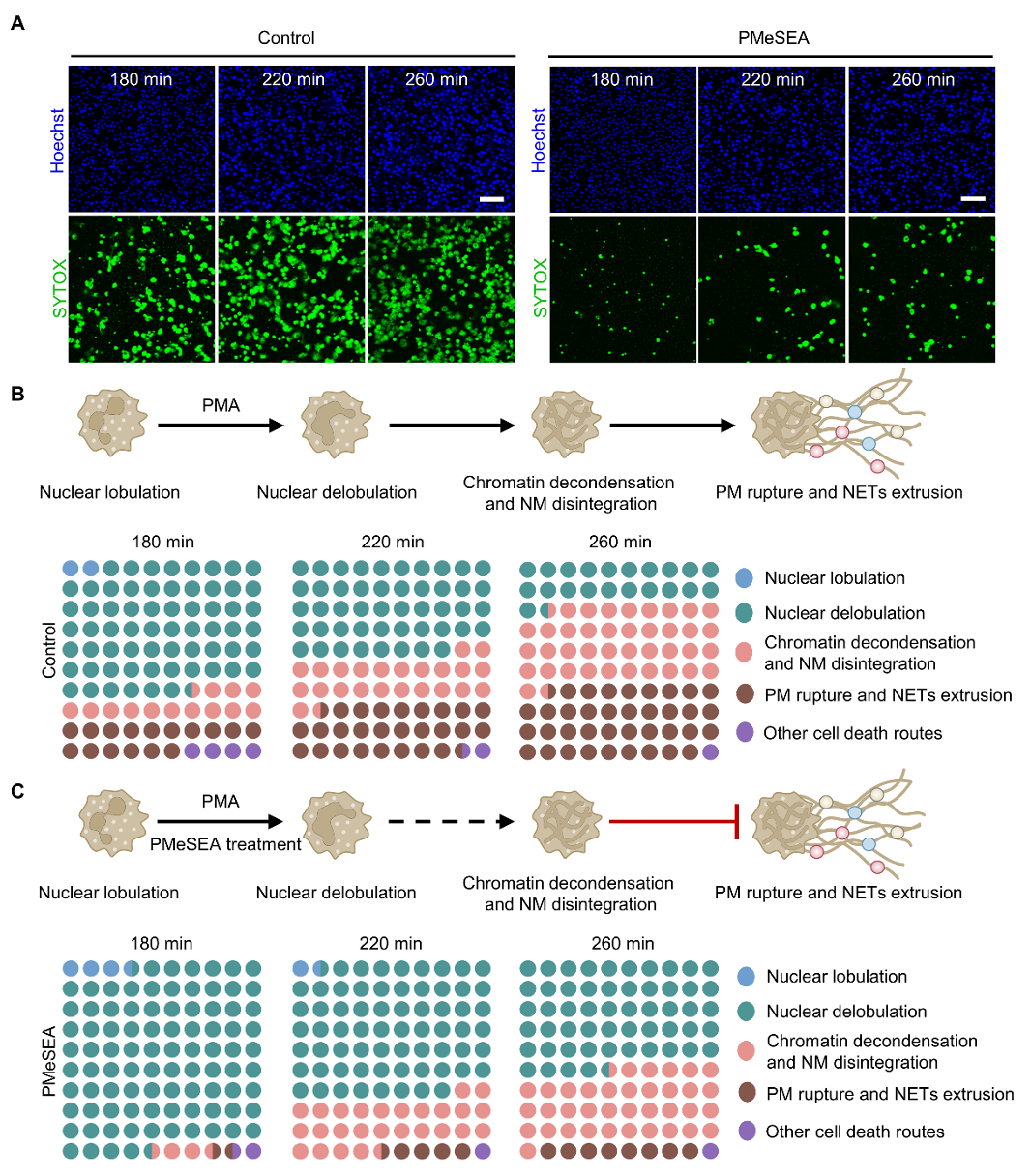
图3 PMeSEA抑制炎症中性粒细胞NETs的释放
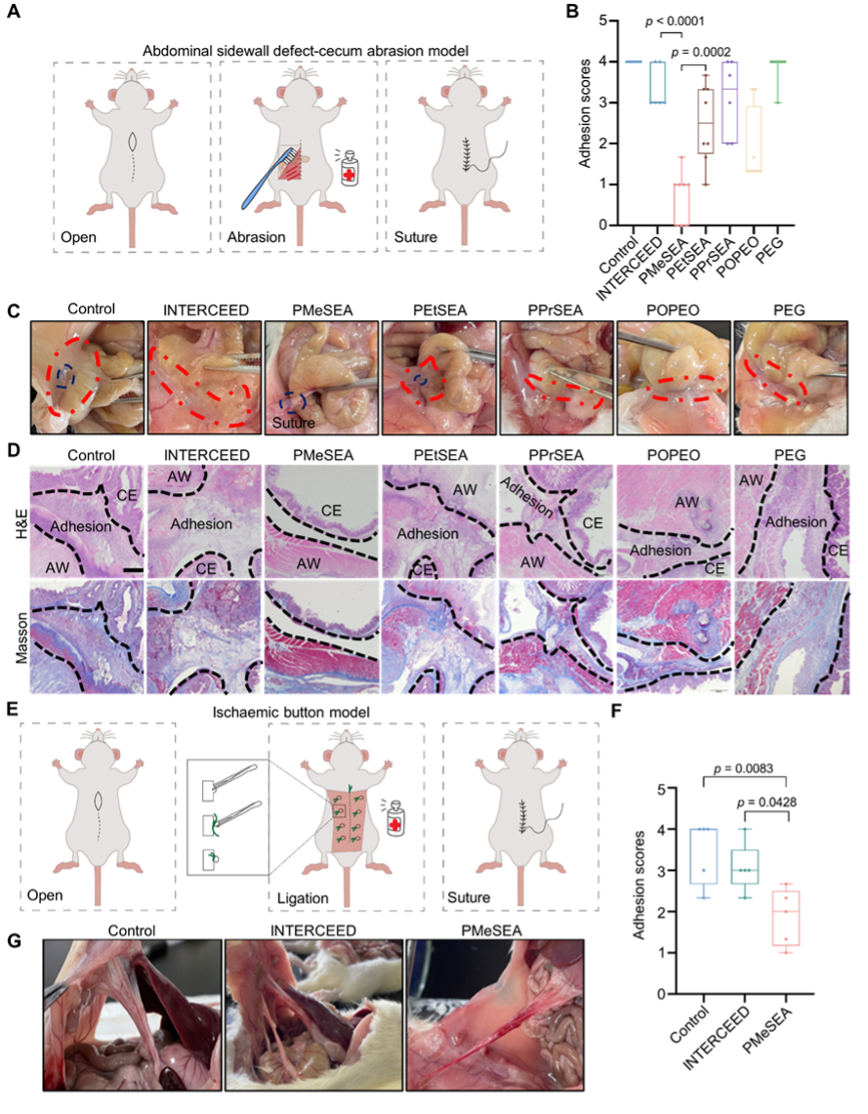
图4 PMeSEA有效抑制术后粘连的发生
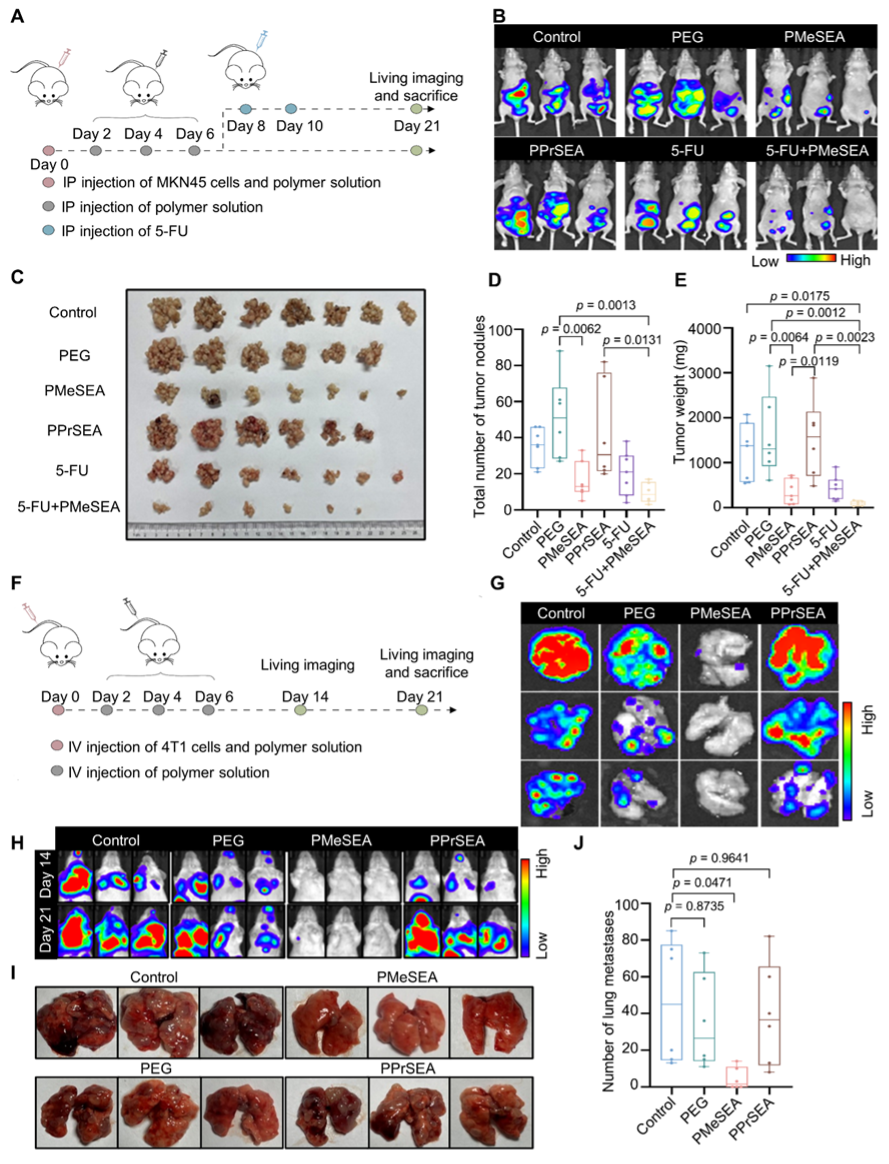
图5 PMeSEA抑制肿瘤腹腔转移和肺转移
本研究开发了系列具有生物活性的超亲水性亚砜高分子材料,并首次揭示了其有着选择性HOCl捕获、NETs抑制等内源生物活性,能显著抑制多种术后并发症的产生,为新型生物医用高分子材料的开发提供新的思路。已有多项相关专利申请并授权,同时研究者们也正积极探索该亚砜类生物材料在其他疾病中的应用,并尝试对其分子机理进行进一步阐明。
浙江大学基础医学院王佳峰、浙江大学医学院附属第四医院王烨淳为该论文的共同第一作者。浙江大学基础医学院周泉、刘祥瑞、周天华为该论文的通讯作者,本研究受到国家自然基金委 (52173141, 82102192, 32101128, 21975218)相关基金的资助。



