生物功能性肽广泛参与信号传导、免疫调节与疾病进程,在生物医药中具有重要潜力。随着组学技术发展,其系统鉴定与功能解析为精准医学提供了新机遇。但肽类药物仍受限于体内不稳定、生物利用度低、难以跨膜及缺乏精准靶向等问题。现有化学修饰与纳米载体虽能改善肽类药物性能,却仍存在免疫原性增强、毒性累积及递送效率不足等挑战。因此,如何在稳定性、靶向性、细胞摄取与可控释放之间取得平衡,是推动肽类药物临床转化的重要挑战。
林爱福教授团队前期在微肽研究与转化方面开展系列研究,在人类胃癌样本中率先鉴定近万个基于非编码RNA的新型微肽,并结合深度学习绘制人类微肽功能谱图(Cell Research,封面报道)。揭示线粒体微肽 MRPIP 调控翻译机器组装并抑制肝癌进程,发现天然微肽药物前体(Molecular Cell,封面报道)。基于免疫检查点分子翻译后修饰,开发新型抗肿瘤先导药物 PTPR(Nature Communications)。相关成果已整合至自主构建的“人类微肽谱图”(HMPA, hmpa.zju.edu.cn),并持续更新(Briefings in Bioinformatics), 为精准医学、后基因组治疗及高效肽类递送体系开发提供数据支撑。

2025年8月11日,浙江大学生命科学学院林爱福等团队在Advanced Science杂志在线发表题为PD-L1-Targeting Biomimetic Photoresponsive Thermosensitive Liposomes for Triple-Negative Breast Cancer的研究论文,研究开发了一种多功能仿生纳米肽类药物递送体系PGFP+,整合三大模块:经氟化修饰的 PD-L1 抑制肽 PTPR,提高稳定性与胞内递送效率;光敏剂 ICG 在近红外光下触发脂质体相变,实现药物释放并通过 42 ℃ 光热效应诱导免疫原性细胞死亡,激活全身免疫应答;血小板膜伪装延长循环、逃避免疫清除并依赖 CD62p/CD44 实现精准靶向。
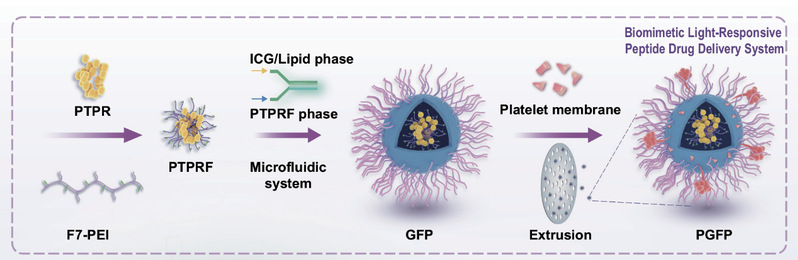
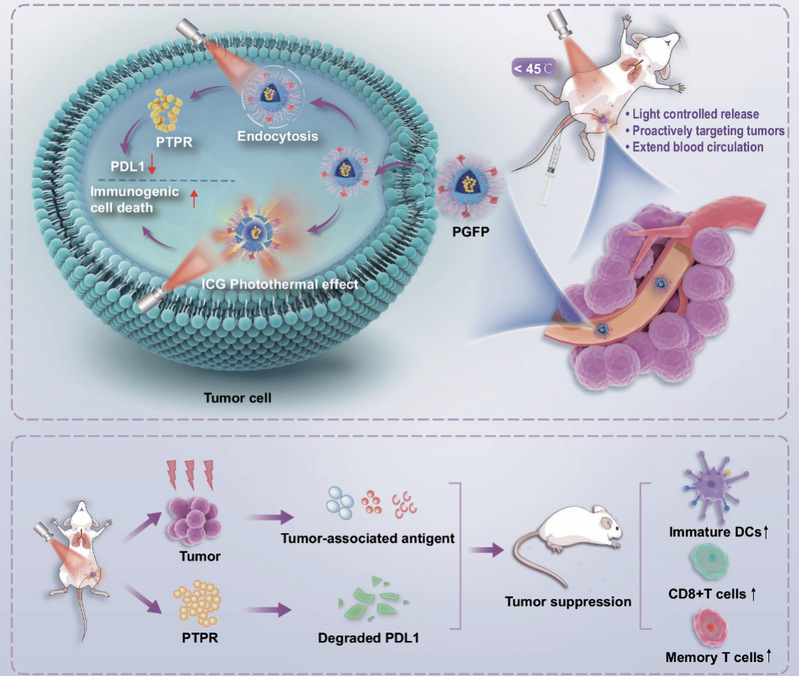
在三阴性乳腺癌原位、远处及转移模型中,PGFP+有效抑制肿瘤进展,增强 T 细胞浸润,促进树突状细胞成熟并下调肿瘤PD-L1表达,诱导持久免疫记忆,防止复发。温和光热疗法避免高温损伤,血小板膜伪装降低脱靶副作用,整体显著提升治疗安全性。
该研究提出集“精准递送+免疫激活”于一体的肽类药物递送策略,为提高免疫肽稳定性、肿瘤靶向性与递送效率提供新思路,为 TNBC 等难治性肿瘤提供新方案。
浙江大学生命科学学院林爱福教授、浙江大学周民教授、刘祥瑞教授、王凯教授为本论文通讯作者。浙江大学生命科学学院谭曼曼、石成瑜、池光熠以及苏心婉为此论文共同第一作者。该工作得到了国家杰出青年科学基金、国家科技创新重大专项等资助。



