全球每年超过150万例的肩袖、交叉韧带等腱骨损伤修复手术,面临一个根本性临床难题:外科缝合虽能实现力学固定,却无法在肌腱(软)与骨骼(硬)之间重建具有生物活性的纤维软骨过渡层。缺失这一关键的“生物接口”,修复组织由瘢痕纤维化胶原替代,直接导致再撕裂率高、功能恢复差。根源在于对腱骨连接处的纤维软骨胶原,其纳米尺度的精确构成及其再生所需的定量化生物材料参数,长期缺乏认知。
近日,浙大基础医学院陈晓和茵梓教授团队联合浙大化学系唐睿康教授、浙大二院沈炜亮主任医师团队,在该领域取得从“原理发现”到“材料创造”的原创性突破。研究团队不仅首次在2-3纳米分辨率下解码了纤维软骨的正常胶原内矿化三维结构,更关键的是,发现了驱动纤维软骨再生的精确无机物含量阈值(33%)。基于此,成功创制出符合该“黄金比例”的仿生矿化胶原支架,在从小鼠、大鼠、兔直至山羊的多物种模型中,逆转瘢痕纤维化胶原沉积,实现了优越的纤维软骨再生与功能恢复,标志着腱骨修复从“机械固定”迈向“生物融合”取得了关键进展。
2025年12月10日,这项研究成果“A Bioinspired mineralized collagen scaffold promotes enthesis healing and activates Gli1 expression in preclinical models” 发表于国际顶级期刊《Science Translational Medicine》。期刊编辑在评价中高度认可其临床转化前景。
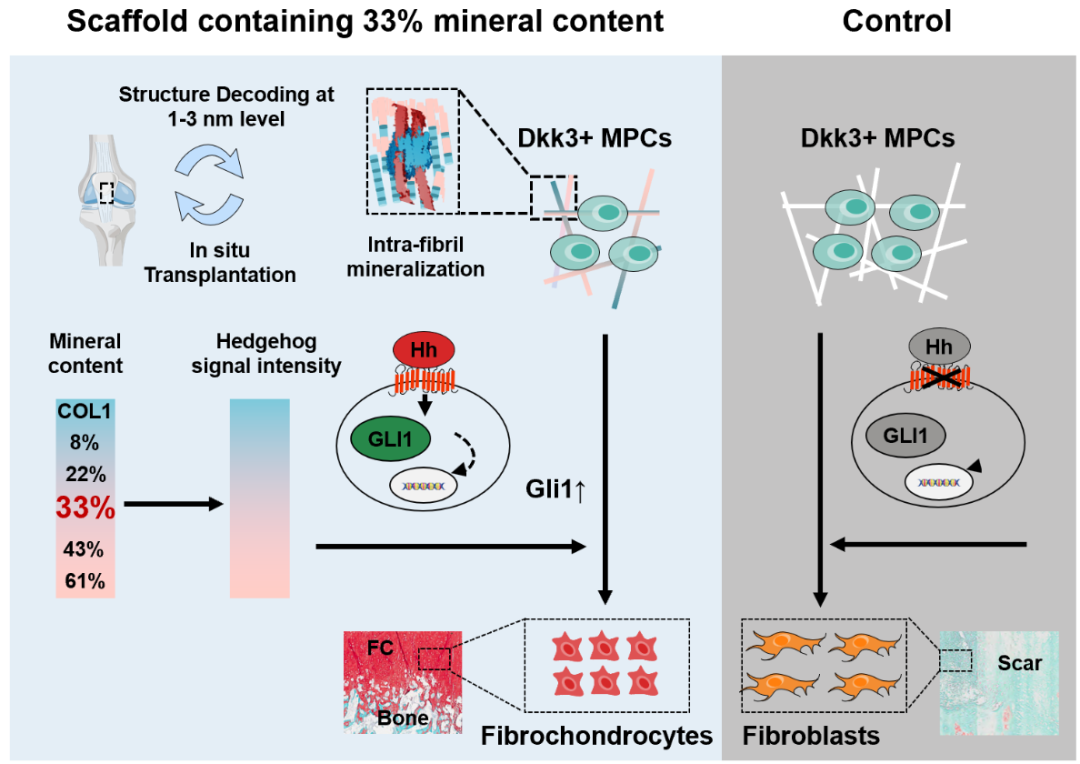
研究团队通过2纳米精度的三维结构解析,首次揭示了腱骨连接处的纤维软骨层中无机物结晶贯穿胶原原纤维内外的半矿化组织特征。基于这一天然结构模板,团队利用磷酸钙纳米簇成功实现了纤维软骨胶原的体内外仿生重构。该胶原支架原位激活内源性Gli1+腱骨祖细胞,促进小鼠、大鼠、兔、山羊等多种模型动物的纤维软骨再生。其中,山羊模型中该支架实现了84%的纤维软骨恢复率,显著提升其运动极限能力。
1. 核心突破:首次于纳米尺度定义纤维软骨的“胶原内矿化”结构蓝图
本研究利用聚焦离子束扫描电镜(FIB-SEM)三维重构等技术,以2-3纳米空间分辨率,精准解析了大型动物及人类纤维软骨的胶原微观构造。团队首次清晰揭示天然纤维软骨中的矿物晶体,是以一种特异性贯穿于胶原原纤维内部的方式有序排列,形成独特的“半矿化”状态。这一定量化的结构蓝图,为仿生材料设计提供了纳米级精确的模板(图1),将仿生尺度从微米级推入纳米时代。
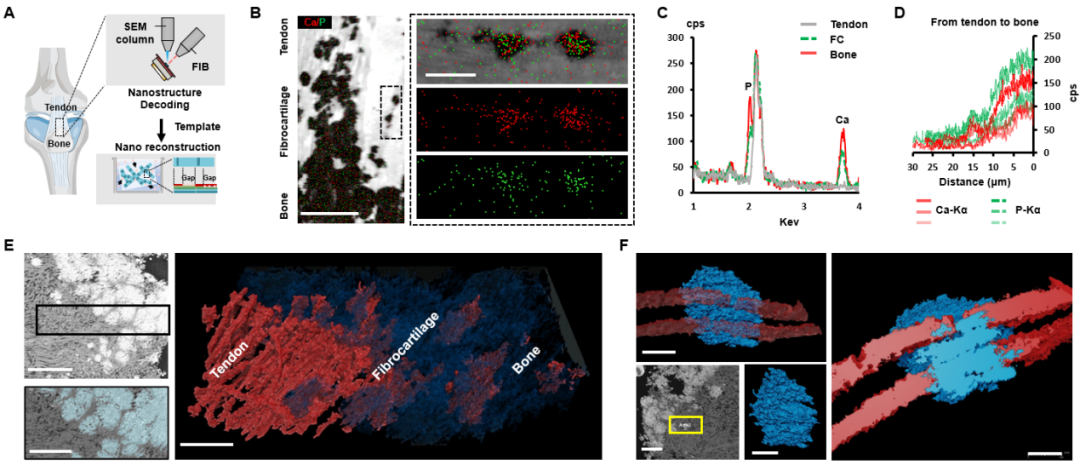
图1:腱骨纤维软骨组织纳米三维影像
2. 概念与材料创新:发现“33%矿化含量”这一再生黄金定律,并实现可控制备
基于结构解码,团队重塑胶原原纤维,矿物贯穿胶原内外,构建了系列无机物含量精准可控的仿生矿化胶原支架(图2)。在此基础上,本研究提出了定量再生概念:纤维软骨的再生存在一个最优的“矿化窗口”。通过系统的体外筛选,团队首次发现当无机物含量精准控制在33%(33MC)时,胶原纤维最能诱导干细胞向纤维软骨分化,而非形成瘢痕纤维或过度骨化(图2)。实现了从“知道该做什么”到“能做出来”的关键跨越。
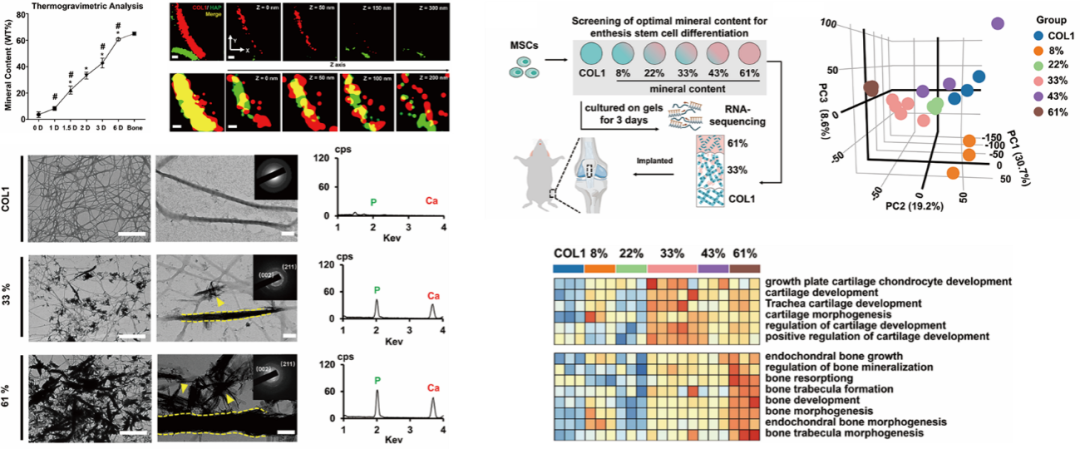
图2:体外重构无机物贯穿胶原原纤维内外,确定33%矿化黄金比例
3. 机制创新:阐明“材料信号(33%矿化)→ 细胞解码(Gli1表达)→ 命运决定(纤维软骨分化)”的全新机制
为进一步阐明33MC胶原支架促进再生的机制,研究团队利用单细胞测序解析体内腱骨再生微环境细胞,发现支架以矿化依赖性方式调控Hedgehog信号通路强度,进而特异性上调关键转录因子Gli1 在间充质祖细胞中的表达,驱动其向纤维软骨细胞分化(图3)。利用谱系追踪技术证实,Gli1+细胞在支架作用下被激活并定向分化为纤维软骨细胞,参与组织再生(图3)。
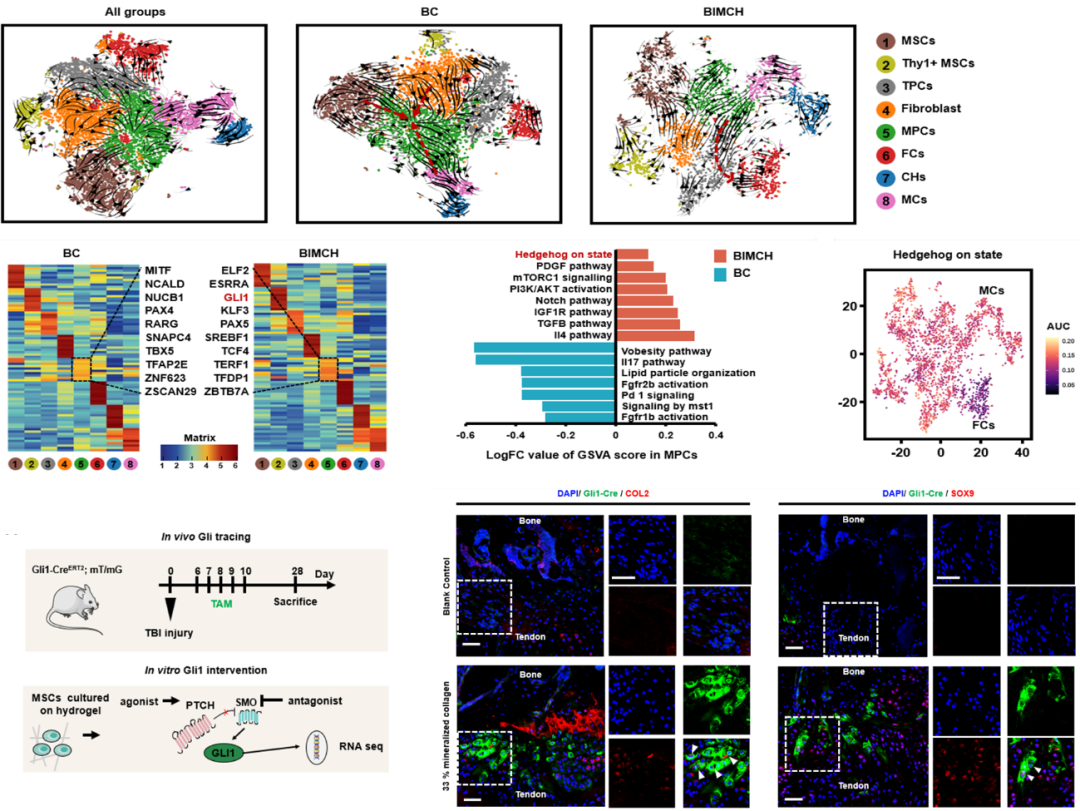
图3:33MC调控间充质祖细胞中Gli1的表达,驱动其向纤维软骨细胞分化
4. 转化创新:大型动物模型系统性验证,搭建从实验室到产业的标准化桥梁
研究的最终指向是临床价值。在兔模型中进行“头对头”比较中,33MC支架的纤维软骨再生宽度恢复率达82%(图4)。在山羊临床前模型中,其修复效果更是远超现有临床标准,将纤维软骨恢复率从几乎为0提升至84%,并显著提升了动物的运动极限能力(图4)。
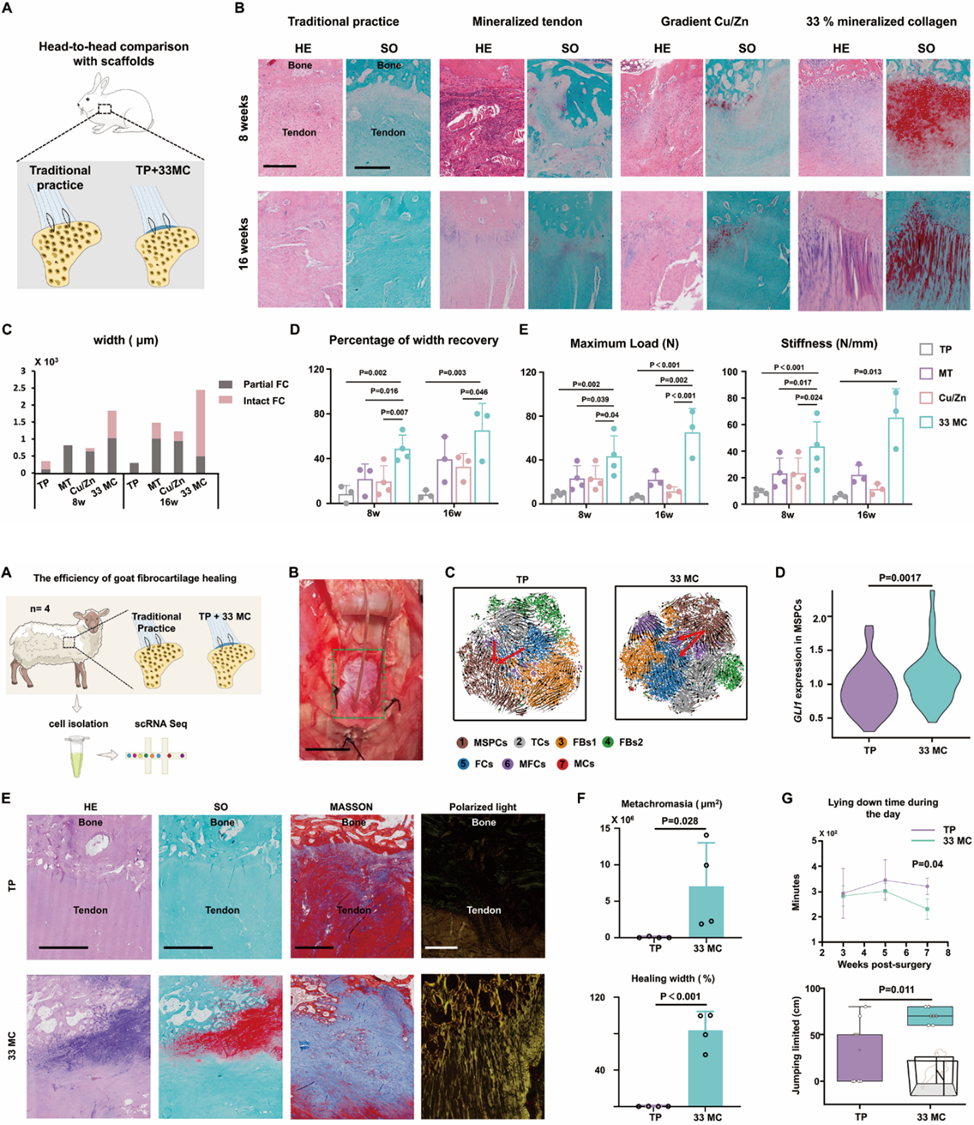
图4: 33MC在兔和山羊腱骨损伤模型中的疗效
为实现从实验室走向规模化生产,团队已建立标准化生产策略,采用符合GMP标准的胶原原料,并开发了自动化、标准化生产设备(特别感谢浙江大学贺永教授团队),构建了稳定的支架制备工艺,为核心技术的专利转化与产业化奠定了坚实基础。其中该项核心技术——“一种仿生矿化胶原膜及其制备方法和在制备医用材料中的应用”专利,于近期在良渚实验室成功实现转化,完成独家授权(贤石生物科技有限公司),标志着这项源于浙江大学与良渚实验室的基础研究成果,正式驶入产品化与临床应用的快车道。

图5 转化签约仪式
浙大二院骨科主治医师张涛为本文第一作者,浙江大学滨江研究院博后雷庭筠、浙江大学医学院韩杰,浙江省人民医院康复科特聘研究员陈扬武为共同第一作者。浙大基础医学院陈晓教授,浙大化学系唐睿康教授,浙大基础医学院茵梓教授,浙大二院骨科沈炜亮主任为该文的通讯作者。本研究得到了国家重点研发计划、国家自然科学基金和浙江省“尖兵领雁+X”研发公关计划等的支持。



