内质网是蛋白质折叠与修饰的关键场所。高温等逆境胁迫下,内质网中容易积累错误折叠的蛋白质,从而触发未折叠蛋白应答(Unfold protein response, UPR)以及内质网相关蛋白降解(ER associated protein degradation, ERAD)机制,以降低内质网错误折叠蛋白积累的水平。信号肽肽酶(SPPs)在哺乳动物的信号肽膜内蛋白水解中发挥着关键作用。然而,它们在植物中的功能仍知之甚少。
5月7日,生命科学学院刘建祥教授团队在Nature Communications在线发表了题为“Signal peptide peptidase like proteases OsSPPL1 and OsSPPL2 facilitate ER-associated protein degradation in rice”的研究论文,揭示了两个类信号肽肽酶OsSPPL1和OsSPPL2在水稻ERAD中的关键功能及其与高温抗性的关系。

OsSPPL1/2对维持内质网蛋白质稳态至关重要
OsbZIP50是UPR途径核心调控因子。OsbZIP50突变体中OsSPPL1/2均不再受衣霉素(Tunicamycin,TM)诱导。Effector-Report,ChIP-qPCR,EMSA等实验进一步说明OsbZIP50通过结合OsSPPL1/2启动子序列直接调控内质网胁迫下两者的表达。经衣霉素处理,OsSPPL1/2双突体表现出生长缺陷,根长、株高、鲜重都显著下降的表型,而过表达植株则抗性增强(图一)。转录组数据表明基因OsSPPL1/2的缺失严重影响内质网蛋白质加工及折叠途径。上述结果充分说明OsSPPL1/2是内质网胁迫的响应因子,在维持内质网稳态方面发挥正向调控的功能。
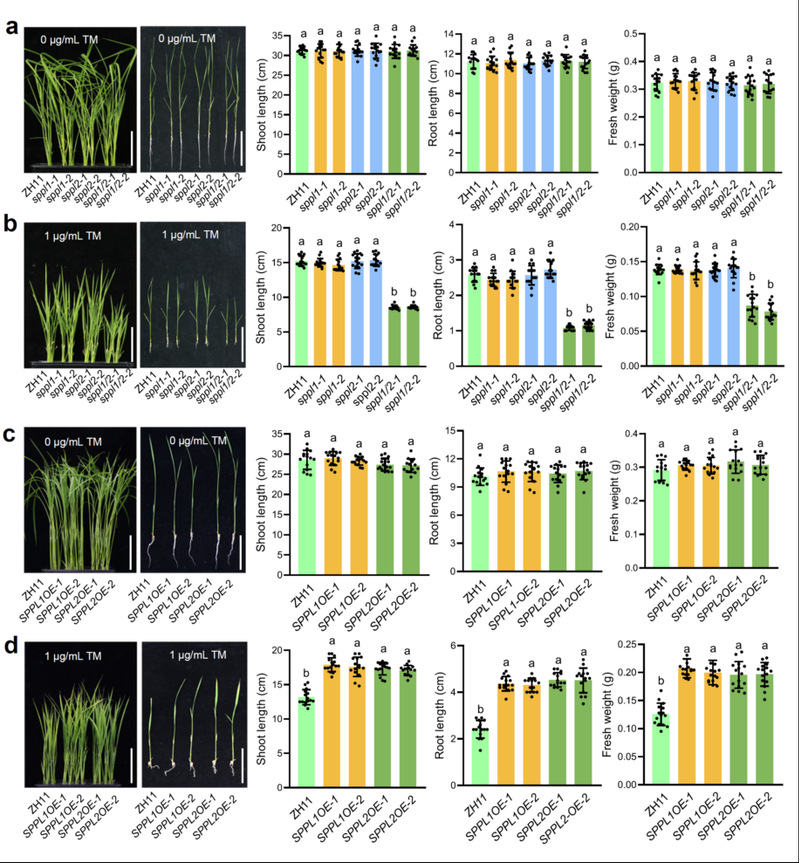
图一 OsSPPL1/2调控内质网蛋白质稳态
通过膜系统酵母双杂交发现OsSPPL1/2与ERAD途径的HRD1复合体成员DER1,DER2蛋白互作,并通过Pull-down,BiFC进行了验证。同时,团队开发了一个全新的ERAD底物ZmFL2m-GFP,将玉米Floury2的信号肽切割位点进行定点突变(ZmFL2m)并融合GFP,使其滞留于内质网膜,诱导内质网胁迫。烟草瞬时表达OsSPPL1/2可显著降低ZmFL2m-GFP蛋白丰度。将ZmFL2m-GFP导入OsSPPL1/2双突或过表达材料中,OsSPPL1/2双突变体中ZmFL2m-GFP过度累积,过表达OsSPPL1/2有助于降解ZmFL2m-GFP(图二)。上述结果均说明OsSPPL1/2可促进ZmFL2m-GFP底物降解,从而缓解内质网胁迫。
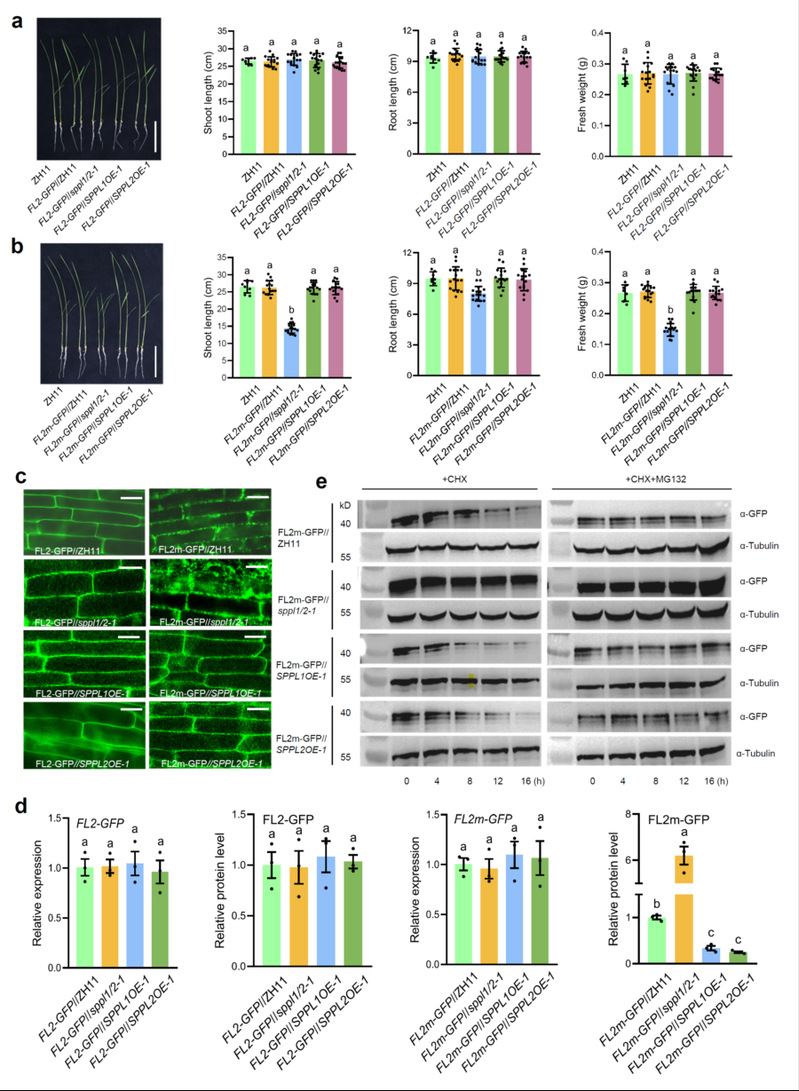
图二 OsSPPL1/2参与ZmFL2m-GFP降解
OsSPPL1/2正向调控水稻高温抗性
高温环境下蛋白往往不能正确折叠或者直接变性,导致错误折叠蛋白累积,引起内质网胁迫。团队进一步研究了OsSPPL1/2在调控水稻高温抗性中功能。幼苗期高温处理,OsSPPL1/2双突存活率显著降低,过表达植株则抗性增强。生殖期阶段高温处理,OsSPPL1/2过表达植株也表现出更高的结实率(图三)。田间试验结果也表明OsSPPL1/2过表达植株有更强的高温抗性和产量。上述结果说明OsSPPL1/2具有水稻高温抗性育种的潜力。
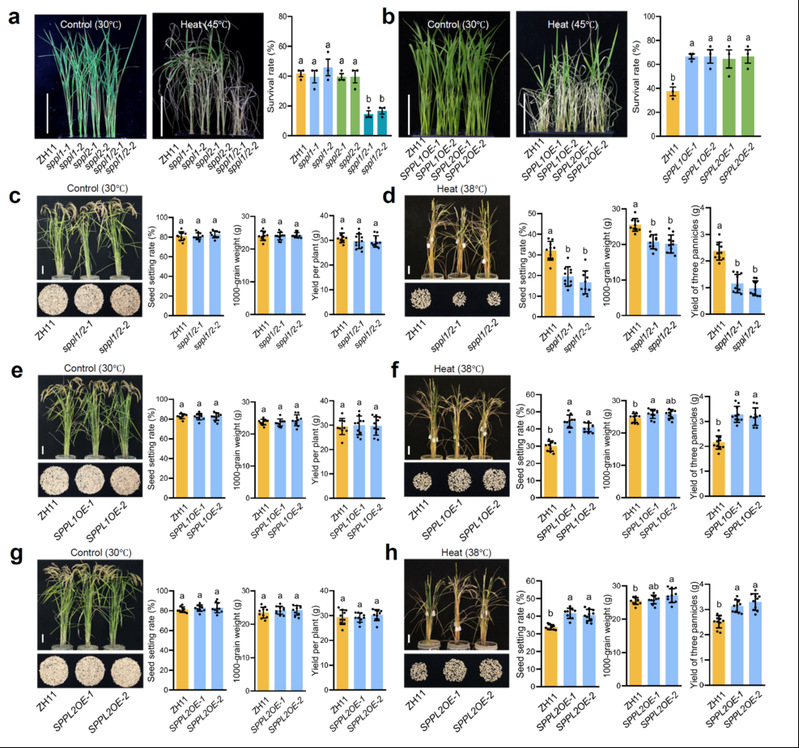
图三 OsSPPL1/2正向调控水稻高温抗性
综上所述,该研究揭示了植物ERAD途径的新成员,阐明了OsSPPL1/2在调控内质网蛋白稳态方面的作用机制(图四),强调了ERAD在植物耐热性中的重要性,为水稻高温抗性育种提供理论基础。
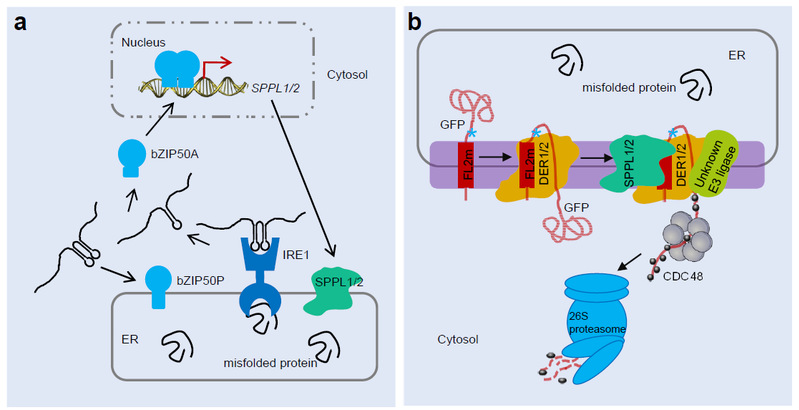
图四 OsSPPL1/2调控ERAD的分子机制模式图
浙江大学生命科学学院植物所特聘研究员芦海平为第一作者,研究生徐舰航、常嘉馨、罗惠丹等参与了该项研究工作。浙江大学生命科学学院刘建祥教授和芦海平研究员为论文通讯作者。该研究得到了国家重点研发计划、国家自然科学基金等项目资助。



